





































 © 2004 - 2015 Pianeta Marte.net - All right reserved
© 2004 - 2015 Pianeta Marte.net - All right reserved
 Sono quasi 40 anni ormai che si discute della missione VIKING ed in particolare degli esperimenti che avrebbero dovuto
Sono quasi 40 anni ormai che si discute della missione VIKING ed in particolare degli esperimenti che avrebbero dovuto provare o escludere la presenza di vita su Marte. Questi esperimenti erano concepiti per rilevare attività biologiche
provare o escludere la presenza di vita su Marte. Questi esperimenti erano concepiti per rilevare attività biologiche anche minime usando tre metodiche differenti, una delle quali (il labeled release (LR) o rilascio marcato) ha dato esiti
anche minime usando tre metodiche differenti, una delle quali (il labeled release (LR) o rilascio marcato) ha dato esiti decisamente positivi! Il Dottor Gilbert V. Levin, ideatore e curatore dell'esperimento LR, ha sempre sostenuto la positività degli
decisamente positivi! Il Dottor Gilbert V. Levin, ideatore e curatore dell'esperimento LR, ha sempre sostenuto la positività degli esiti dell'esperimento, in netto disaccordo con i vertici della NASA che invece hanno completamente rigettato ogni spiegazione di
esiti dell'esperimento, in netto disaccordo con i vertici della NASA che invece hanno completamente rigettato ogni spiegazione di tipo biologico a causa del mancato rilevamento di composti organici da parte del gascromatografo.
tipo biologico a causa del mancato rilevamento di composti organici da parte del gascromatografo. In realtà, con gli anni, saltò fuori che il gascromatografo aveva rilevato clorometano e diclorometano, ma che furono ritenuti
In realtà, con gli anni, saltò fuori che il gascromatografo aveva rilevato clorometano e diclorometano, ma che furono ritenuti una “contaminazione terrestre” dovuta probabilmente al detergente usato per sterilizzare le sonde. Vorrei far notare che tanto il
una “contaminazione terrestre” dovuta probabilmente al detergente usato per sterilizzare le sonde. Vorrei far notare che tanto il clorometano quanto il diclorometano sono estremamente volatili; come potevano essere sopravvissuti sulle sonde a parecchi
clorometano quanto il diclorometano sono estremamente volatili; come potevano essere sopravvissuti sulle sonde a parecchi mesi di viaggio nel vuoto cosmico???
mesi di viaggio nel vuoto cosmico??? Da notare anche il fatto dimostrato che copie di quel gascromatografo fallirono il rilevamento di composti organici anche su
Da notare anche il fatto dimostrato che copie di quel gascromatografo fallirono il rilevamento di composti organici anche su campioni terrestri a carica batterica conosciuta. Nonostante ciò, il mancato rilevamento di composti organici è rimasto fino ad
campioni terrestri a carica batterica conosciuta. Nonostante ciò, il mancato rilevamento di composti organici è rimasto fino ad oggi l'unico appiglio tecnico per annullare la validità dell'esito positivo dell'esperimento LR. Oltretutto anche gli altri due
oggi l'unico appiglio tecnico per annullare la validità dell'esito positivo dell'esperimento LR. Oltretutto anche gli altri due esperimenti biologici, lo scambio gassoso (Gas Exchange o GEX) e il rilascio pirolitico (Pyrolytic Release o PR), diedero esiti
esperimenti biologici, lo scambio gassoso (Gas Exchange o GEX) e il rilascio pirolitico (Pyrolytic Release o PR), diedero esiti interessanti tutt'altro che semplicemente negati, come invece affermano molti sedicenti “divulgatori”.
interessanti tutt'altro che semplicemente negati, come invece affermano molti sedicenti “divulgatori”. Per un'approfondita analisi dei tre esperimenti vi rimandiamo all'articolo: “Le sonde gemelle Viking trovarono la vita su
Per un'approfondita analisi dei tre esperimenti vi rimandiamo all'articolo: “Le sonde gemelle Viking trovarono la vita su Marte?”
Analizzando i vari punti in maniera indipendente si giunge alla conclusione che ci sia stata una volontà precisa di invalidare
Marte?”
Analizzando i vari punti in maniera indipendente si giunge alla conclusione che ci sia stata una volontà precisa di invalidare qualunque spiegazione di natura biologica a tutti i costi. E vediamo anche il perché. Lo scopo degli esperimenti biologici era che,
qualunque spiegazione di natura biologica a tutti i costi. E vediamo anche il perché. Lo scopo degli esperimenti biologici era che, almeno uno dei tre, risultasse positivo. Questa condizione è stata pienamente soddisfatta già dall'esperimento LR e parzialmente
almeno uno dei tre, risultasse positivo. Questa condizione è stata pienamente soddisfatta già dall'esperimento LR e parzialmente anche dagli esperimenti GEX e PR, raggiungendo così l'obiettivo primario preposto.
anche dagli esperimenti GEX e PR, raggiungendo così l'obiettivo primario preposto. Il gascromatografo rilevò clorometano e diclorometano nonostante la sua ridotta sensibilità; copie dello stesso strumento fallirono
Il gascromatografo rilevò clorometano e diclorometano nonostante la sua ridotta sensibilità; copie dello stesso strumento fallirono nel rilevamento di composti organici su campioni prelevati da alcuni deserti terrestri. Ciò significa che il livello di composti organici
nel rilevamento di composti organici su campioni prelevati da alcuni deserti terrestri. Ciò significa che il livello di composti organici sul suolo di Marte è maggiore di quello di alcuni deserti terrestri che comunque ospitano forme di vita. Nonostante ciò, si è
sul suolo di Marte è maggiore di quello di alcuni deserti terrestri che comunque ospitano forme di vita. Nonostante ciò, si è tentato in prima istanza di negare il rilevamento, salvo poi cercare di attribuirlo ad una contaminazione “terrestre”. Questa
tentato in prima istanza di negare il rilevamento, salvo poi cercare di attribuirlo ad una contaminazione “terrestre”. Questa argomentazione analizzata oggi risulta decisamente insostenibile. Intanto non mi risulta che il clorometano e il diclorometano
argomentazione analizzata oggi risulta decisamente insostenibile. Intanto non mi risulta che il clorometano e il diclorometano vengano usati come detergenti o sterilizzanti. Ammesso e non concesso che questi composti fossero presenti al momento del
vengano usati come detergenti o sterilizzanti. Ammesso e non concesso che questi composti fossero presenti al momento del lancio, avrebbero dovuto disperdersi completamente durante il viaggio di andata verso Marte.
lancio, avrebbero dovuto disperdersi completamente durante il viaggio di andata verso Marte. Anche ammettendo la possibilità che una qualche quantità di contaminante sia rimasta sulla sonda, sopravvivendo al viaggio,
Anche ammettendo la possibilità che una qualche quantità di contaminante sia rimasta sulla sonda, sopravvivendo al viaggio, quest’ultima avrebbe dovuto diminuire ad ogni successiva analisi di un nuovo campione. Immaginiamo per esempio di usare un
quest’ultima avrebbe dovuto diminuire ad ogni successiva analisi di un nuovo campione. Immaginiamo per esempio di usare un cucchiaino sporco di miele per raccogliere del sale; la prima cucchiaiata sarà sicuramente la più “sporca” ma, man mano che
cucchiaino sporco di miele per raccogliere del sale; la prima cucchiaiata sarà sicuramente la più “sporca” ma, man mano che andiamo avanti, il cucchiaino stesso tenderà a perdere lo strato di miele fino a rimanere pressoché pulito. Quindi, la “scusa” della
andiamo avanti, il cucchiaino stesso tenderà a perdere lo strato di miele fino a rimanere pressoché pulito. Quindi, la “scusa” della contaminazione terrestre non è per nulla convincente in quanto avrebbero potuto discriminarla ripetendo più volte l'analisi. Risulta
contaminazione terrestre non è per nulla convincente in quanto avrebbero potuto discriminarla ripetendo più volte l'analisi. Risulta quindi evidente la volontà di utilizzare l'esperimento col gascromatografo per invalidare gli altri tre. Infatti per sostenere questa
quindi evidente la volontà di utilizzare l'esperimento col gascromatografo per invalidare gli altri tre. Infatti per sostenere questa debole tesi si è ricorso a spiegazioni fantasiose come la pioggia di super ossidi che avrebbero così sterilizzato continuamente la
debole tesi si è ricorso a spiegazioni fantasiose come la pioggia di super ossidi che avrebbero così sterilizzato continuamente la superficie marziana nonostante gli apporti meteorici. E infatti ben noto che una costante pioggia di meteoriti e comete fornisce un
superficie marziana nonostante gli apporti meteorici. E infatti ben noto che una costante pioggia di meteoriti e comete fornisce un costante apporto di composti organici alla superficie marziana. Inutile aggiungere che ne acqua ossigenata ne qualsivoglia sorta
costante apporto di composti organici alla superficie marziana. Inutile aggiungere che ne acqua ossigenata ne qualsivoglia sorta di super ossido è mai stato identificato sulla superficie marziana.
di super ossido è mai stato identificato sulla superficie marziana. Ci troviamo quindi di fronte ad una serie di teorie farlocche e mai dimostrate che hanno tenuto banco fino ai giorni nostri a
Ci troviamo quindi di fronte ad una serie di teorie farlocche e mai dimostrate che hanno tenuto banco fino ai giorni nostri a sostegno della tesi che la superficie di Marte fosse completamente sterile e priva di composti organici, oltreché estremamente
sostegno della tesi che la superficie di Marte fosse completamente sterile e priva di composti organici, oltreché estremamente ossidante. Una teoria contro dei fatti oggettivi; questo è ciò che la NASA ha usato contro le tesi del dr. Levin. Nessun metodo
ossidante. Una teoria contro dei fatti oggettivi; questo è ciò che la NASA ha usato contro le tesi del dr. Levin. Nessun metodo scientifico può essere invocato a sostegno di questo modus operandi; un esperimento che si prefigge determinati scopi e che li
scientifico può essere invocato a sostegno di questo modus operandi; un esperimento che si prefigge determinati scopi e che li raggiunge è universalmente riconosciuto come “esito positivo”.
raggiunge è universalmente riconosciuto come “esito positivo”.  Per i più coriacei viene in aiuto la missione MSL Curiosity, la quale ha rilevato sia i composti già trovati dalle Viking che una bella
Per i più coriacei viene in aiuto la missione MSL Curiosity, la quale ha rilevato sia i composti già trovati dalle Viking che una bella sfilza di idrocarburi! Come la mettiamo adesso?? Rimarremo tutti devoti alla “Santa Madre NASA” o decideremo finalmente di
sfilza di idrocarburi! Come la mettiamo adesso?? Rimarremo tutti devoti alla “Santa Madre NASA” o decideremo finalmente di aprire gli occhi e accendere i neuroni?
aprire gli occhi e accendere i neuroni?  Ecco una breve descrizione dei composti organici rilevati:
Vista la varietà di composti organici rilevati, vorrei far notare quanto fosse insulsa la teoria dei “Super ossidi” che avrebbero
Ecco una breve descrizione dei composti organici rilevati:
Vista la varietà di composti organici rilevati, vorrei far notare quanto fosse insulsa la teoria dei “Super ossidi” che avrebbero distrutto anche quel po' di composti organici che arrivavano dallo spazio. Visto che anche sulla Luna sono presenti un minimo di
distrutto anche quel po' di composti organici che arrivavano dallo spazio. Visto che anche sulla Luna sono presenti un minimo di composti organici, giustificare la loro totale assenza dalla superficie di Marte ha richiesto veramente un colpo di genio
composti organici, giustificare la loro totale assenza dalla superficie di Marte ha richiesto veramente un colpo di genio eccezionale!
eccezionale! In un documento pubblicato dalla NASA il 30 dicembre 1979 intitolato “Viking magnetic properties experiment - Extended mission
In un documento pubblicato dalla NASA il 30 dicembre 1979 intitolato “Viking magnetic properties experiment - Extended mission results”, disponibile all'indirizzo http://ntrs.nasa.gov/search.jsp?R=19800042219 , si legge:
results”, disponibile all'indirizzo http://ntrs.nasa.gov/search.jsp?R=19800042219 , si legge: “I magneti del retroescavatore sul Viking Lander (VL) 2 furono puliti con successo, in seguito fu eseguito un test praticando
“I magneti del retroescavatore sul Viking Lander (VL) 2 furono puliti con successo, in seguito fu eseguito un test praticando interramenti successivi del retroescavatore pulito nella superficie. La rapida saturazione dei magneti ha confermato le prove
interramenti successivi del retroescavatore pulito nella superficie. La rapida saturazione dei magneti ha confermato le prove risultanti dalla missione primaria, cioè che il minerale magnetico nella superficie marziana è ampiamente distribuito,
risultanti dalla missione primaria, cioè che il minerale magnetico nella superficie marziana è ampiamente distribuito, probabilmente in forma di particelle miste di minerali magnetici e non magnetici. Un'immagine del retroescavatore del VL 2 prese
probabilmente in forma di particelle miste di minerali magnetici e non magnetici. Un'immagine del retroescavatore del VL 2 prese con lo specchio di ingrandimento X4 dimostra la natura granulare del materiale magnetico attratto. La presenza di maghemite e
con lo specchio di ingrandimento X4 dimostra la natura granulare del materiale magnetico attratto. La presenza di maghemite e la sua comparsa come parte del pigmento, o come sottile rivestimento, in tutte le particelle minerali, o nei cristalliti discretamente
la sua comparsa come parte del pigmento, o come sottile rivestimento, in tutte le particelle minerali, o nei cristalliti discretamente e finemente suddivisi e diffusi, sono coerenti con i dati provenienti dagli esperimenti di analisi inorganica e simulazioni di
e finemente suddivisi e diffusi, sono coerenti con i dati provenienti dagli esperimenti di analisi inorganica e simulazioni di laboratorio dei risultati degli esperimenti biologici compiuti su Marte.”.
Il Dottor Levin ha fatto notare in diverse pubblicazioni l'incompatibilità della presenza di materiale magnetizzato con un suolo
laboratorio dei risultati degli esperimenti biologici compiuti su Marte.”.
Il Dottor Levin ha fatto notare in diverse pubblicazioni l'incompatibilità della presenza di materiale magnetizzato con un suolo fortemente ossidante. Un suolo fortemente ossidante distruggerebbe ogni traccia di materiale magnetico che quindi non avrebbe
fortemente ossidante. Un suolo fortemente ossidante distruggerebbe ogni traccia di materiale magnetico che quindi non avrebbe potuto essere catturato dai magneti a bordo del VL2!
potuto essere catturato dai magneti a bordo del VL2! Ma non basta; il clorometano e il diclorometano rilevati dal gascromatografo erano anch'essi incompatibili con un suolo
Ma non basta; il clorometano e il diclorometano rilevati dal gascromatografo erano anch'essi incompatibili con un suolo fortemente ossidante, tanto più se fossero realmente stati un residuo del detergente usato per sterilizzare i due landers! Infatti un
fortemente ossidante, tanto più se fossero realmente stati un residuo del detergente usato per sterilizzare i due landers! Infatti un terreno fortemente ossidante avrebbe distrutto i due composti prima ancora che il gascromatografo iniziasse a scaldare i
terreno fortemente ossidante avrebbe distrutto i due composti prima ancora che il gascromatografo iniziasse a scaldare i campioni di suolo stesso! È totalmente illogico pensare che un terreno in grado di aggredire e distruggere qualunque composto
campioni di suolo stesso! È totalmente illogico pensare che un terreno in grado di aggredire e distruggere qualunque composto organico proveniente dallo spazio non sia poi in grado di distruggere le deboli tracce lasciate da un detergente!
organico proveniente dallo spazio non sia poi in grado di distruggere le deboli tracce lasciate da un detergente!  Per decenni, schiere di giornalisti scientifici e divulgatori, hanno strombazzato la negatività degli esperimenti biologici compiuti
Per decenni, schiere di giornalisti scientifici e divulgatori, hanno strombazzato la negatività degli esperimenti biologici compiuti dalle sonde Viking, senza mai entrare minimamente nel dettaglio dei singoli esperimenti e senza mai palesare il benché minimo
dalle sonde Viking, senza mai entrare minimamente nel dettaglio dei singoli esperimenti e senza mai palesare il benché minimo dubbio al riguardo! È questo il modo di fare giornalismo??? Riportare una notizia senza un minimo di verifica??? Si fa un gran
dubbio al riguardo! È questo il modo di fare giornalismo??? Riportare una notizia senza un minimo di verifica??? Si fa un gran parlare di par condicio, ma chi di voi “Giornalari scientifici” si è mai sognato di esporre anche la tesi del Dottor Gilbert V. Levin in
parlare di par condicio, ma chi di voi “Giornalari scientifici” si è mai sognato di esporre anche la tesi del Dottor Gilbert V. Levin in contrapposizione a quella della NASA???
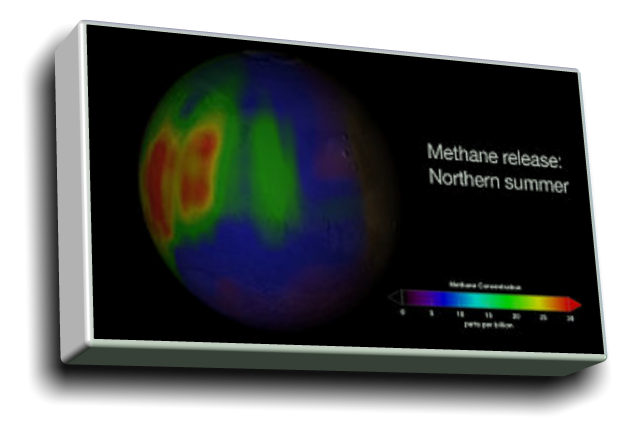
contrapposizione a quella della NASA??? Ultima, ma non per importanza, la questione del metano su Marte come ulteriore prova a sostegno della tesi della vita su Marte.
Ultima, ma non per importanza, la questione del metano su Marte come ulteriore prova a sostegno della tesi della vita su Marte. C'è chi sostiene la sua origine biologica e chi sostiene l'origine geologica o abiogenica, senza di fatto arrivare ad una
C'è chi sostiene la sua origine biologica e chi sostiene l'origine geologica o abiogenica, senza di fatto arrivare ad una conclusione!
conclusione! Ancora una volta, nessuno ci spiega che il vero problema non è da dove arriva il metano ma piuttosto come fa a sparire
Ancora una volta, nessuno ci spiega che il vero problema non è da dove arriva il metano ma piuttosto come fa a sparire così velocemente!! Infatti è stato dimostrato che il metano dovrebbe resistere circa 300 anni nell'atmosfera marziana prima di
così velocemente!! Infatti è stato dimostrato che il metano dovrebbe resistere circa 300 anni nell'atmosfera marziana prima di disgregarsi e/o reagire con altre sostanze; ma allora come mai lo si vede sparire nell'arco di mesi, a volte settimane o addirittura
disgregarsi e/o reagire con altre sostanze; ma allora come mai lo si vede sparire nell'arco di mesi, a volte settimane o addirittura giorni? Cos'è in grado di distruggere grandi quantità di metano in così poco tempo?
giorni? Cos'è in grado di distruggere grandi quantità di metano in così poco tempo? Ovviamente nessuno si azzarda a sollevare la questione, visto che in questo caso non ci sarebbero le due classiche fazioni
Ovviamente nessuno si azzarda a sollevare la questione, visto che in questo caso non ci sarebbero le due classiche fazioni opposte da lasciare scannare eternamente l'una contro l'altra ma solo un'unica risposta: batteri metanotrofi!!! Proprio così,
opposte da lasciare scannare eternamente l'una contro l'altra ma solo un'unica risposta: batteri metanotrofi!!! Proprio così, perché tutti i processi chimico-fisici conosciuti in grado di distruggere il metano eventualmente immesso nell'atmosfera marziana,
perché tutti i processi chimico-fisici conosciuti in grado di distruggere il metano eventualmente immesso nell'atmosfera marziana, anche se sommati insieme, non riescono far prima dei 300 anni citati prima, quindi in questo caso non ci si può appellare ad altro
anche se sommati insieme, non riescono far prima dei 300 anni citati prima, quindi in questo caso non ci si può appellare ad altro se non ai batteri metanotrofi, ovvero batteri che si nutrono di metano.
se non ai batteri metanotrofi, ovvero batteri che si nutrono di metano. Non credo proprio che simili osservazioni potranno giungere facilmente all'attenzione dell'opinione pubblica, visto che i Media
Non credo proprio che simili osservazioni potranno giungere facilmente all'attenzione dell'opinione pubblica, visto che i Media preferiscono dedicarsi servilmente a propagandare le sole versioni “ufficiali” somministrate dalla NASA e dall'ESA in maniera
preferiscono dedicarsi servilmente a propagandare le sole versioni “ufficiali” somministrate dalla NASA e dall'ESA in maniera totalmente acritica!!! Vorrei tanto avere la possibilità di intervistare pubblicamente almeno uno di quei “geni” che per decenni
totalmente acritica!!! Vorrei tanto avere la possibilità di intervistare pubblicamente almeno uno di quei “geni” che per decenni hanno tenuto banco con le loro teorie assurde come quella dei super ossidi! Evidentemente loro hanno scoperto il vaccino contro
hanno tenuto banco con le loro teorie assurde come quella dei super ossidi! Evidentemente loro hanno scoperto il vaccino contro la vergogna... che magari viene proprio da Marte!
la vergogna... che magari viene proprio da Marte! Pubblicazioni ufficiali di riferimento:
2014 "MARS: Dead or Alive?" Gilbert V. Levin, Arizona State University and Patricia Ann Straat NIH (Ret.) Presented at Mars
Pubblicazioni ufficiali di riferimento:
2014 "MARS: Dead or Alive?" Gilbert V. Levin, Arizona State University and Patricia Ann Straat NIH (Ret.) Presented at Mars Society Convention, League City, TX, August 8, 2014
Society Convention, League City, TX, August 8, 2014 2015 "Mars methane detection and variability at Gale crater" Christopher R. Webster, Paul R. Mahaffy, Sushil K. Atreya, Gregory
2015 "Mars methane detection and variability at Gale crater" Christopher R. Webster, Paul R. Mahaffy, Sushil K. Atreya, Gregory J. Flesch, Michael A. Mischna, Pierre-Yves Meslin, Kenneth A. Farley, Pamela G. Conrad, Lance E. Christensen, Alexander A.
J. Flesch, Michael A. Mischna, Pierre-Yves Meslin, Kenneth A. Farley, Pamela G. Conrad, Lance E. Christensen, Alexander A. Pavlov, Javier Martín-Torres,, María-Paz Zorzano, Timothy H. McConnochie, Tobias Owen, Jennifer L. Eigenbrode, Daniel P.
Pavlov, Javier Martín-Torres,, María-Paz Zorzano, Timothy H. McConnochie, Tobias Owen, Jennifer L. Eigenbrode, Daniel P. Glavin, Andrew Steele, Charles A. Malespin, P. Douglas Archer Jr., Brad Sutter, Patrice Coll, Caroline Freissinet, Christopher P.
Glavin, Andrew Steele, Charles A. Malespin, P. Douglas Archer Jr., Brad Sutter, Patrice Coll, Caroline Freissinet, Christopher P. McKay, John E. Moores, Susanne P. Schwenzer, John C. Bridges, Rafael Navarro-Gonzalez, Ralf Gellert, Mark T. Lemmon, the
McKay, John E. Moores, Susanne P. Schwenzer, John C. Bridges, Rafael Navarro-Gonzalez, Ralf Gellert, Mark T. Lemmon, the MSL Science Team
MSL Science Team 2014 "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D. P. Glavin, P. R.
2014 "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D. P. Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et
Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et al.
al. 2014 "Volatile and Organic Compositions of Sedimentary Rocks in Yellowknife Bay, Gale Crater, Mars" D. W. Ming, P. D. Archer
2014 "Volatile and Organic Compositions of Sedimentary Rocks in Yellowknife Bay, Gale Crater, Mars" D. W. Ming, P. D. Archer Jr., D. P. Glavin, J. L. Eigenbrode, H. B. Franz, B. Sutter, A. E. Brunner, J. C. Stern, C. Freissinet, A. C. McAdam, P. R. Mahaffy,
Jr., D. P. Glavin, J. L. Eigenbrode, H. B. Franz, B. Sutter, A. E. Brunner, J. C. Stern, C. Freissinet, A. C. McAdam, P. R. Mahaffy, M. Cabane, P. Coll, J. L. Campbell, S. K. Atreya, P. B. Niles, J. F. Bell III, D. L. Bish, W. B. Brinckerhoff, A. Buch, P. G. Conrad,
M. Cabane, P. Coll, J. L. Campbell, S. K. Atreya, P. B. Niles, J. F. Bell III, D. L. Bish, W. B. Brinckerhoff, A. Buch, P. G. Conrad, D. J. Des Marais, B. L. Ehlmann, A. G. Fairén, K. Farley, G. J. Flesch, P. Francois, R. Gellert, J. A. Grant, J. P. Grotzinger, S.
D. J. Des Marais, B. L. Ehlmann, A. G. Fairén, K. Farley, G. J. Flesch, P. Francois, R. Gellert, J. A. Grant, J. P. Grotzinger, S. Gupta, K. E. Herkenhoff, J. A. Hurowitz, L. A. Leshin, K. W. Lewis, S. M. McLennan, K. E. Miller, J. Moersch, R. V. Morris, R.
Gupta, K. E. Herkenhoff, J. A. Hurowitz, L. A. Leshin, K. W. Lewis, S. M. McLennan, K. E. Miller, J. Moersch, R. V. Morris, R. Navarro-González, A. A. Pavlov, G. M. Perrett, I. Pradler, S. W. Squyres, R. E. Summons, A. Steele, E. M. Stolper, D. Y.
Navarro-González, A. A. Pavlov, G. M. Perrett, I. Pradler, S. W. Squyres, R. E. Summons, A. Steele, E. M. Stolper, D. Y. Sumner, C. Szopa, S. Teinturier, M. G. Trainer, A. H. Treiman, D. T. Vaniman, A. R. Vasavada, C. R. Webster, J. J. Wray, R. A.
Sumner, C. Szopa, S. Teinturier, M. G. Trainer, A. H. Treiman, D. T. Vaniman, A. R. Vasavada, C. R. Webster, J. J. Wray, R. A. Yingst, MSL Science Team
Yingst, MSL Science Team 2010 "Reanalysis of the Viking results suggests perchlorate and organics at midlatitudes on Mars" Rafael Navarro‐González,
2010 "Reanalysis of the Viking results suggests perchlorate and organics at midlatitudes on Mars" Rafael Navarro‐González, Edgar Vargas, José de la Rosa, Alejandro C. Raga, and Christopher P. McKay
Edgar Vargas, José de la Rosa, Alejandro C. Raga, and Christopher P. McKay

 Gascromatogramma del campione CB-3.
Gascromatogramma del campione CB-3.  1: clorometano, 2: diclorometano, 3: triclorometano, 4: tetracloruro di carbonio, 5: dicloroetane, 6: dicloropropano,
1: clorometano, 2: diclorometano, 3: triclorometano, 4: tetracloruro di carbonio, 5: dicloroetane, 6: dicloropropano,  7: diclorobutano, 8: clorobenzene.
7: diclorobutano, 8: clorobenzene. Tratto da "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D.P.
Tratto da "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D.P. Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B.
Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et al.
Franz, A. Steele et al.
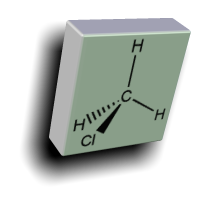

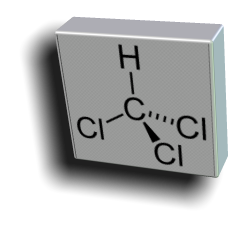



 Il clorometano, detto anche metilcloruro o cloruro di metile (o con le
Il clorometano, detto anche metilcloruro o cloruro di metile (o con le sigle R-40 e HCC 40), è un composto chimico che si presenta sotto
sigle R-40 e HCC 40), è un composto chimico che si presenta sotto forma di gas incolore, infiammabile e caratterizzato da un odore
forma di gas incolore, infiammabile e caratterizzato da un odore leggermente dolciastro. In passato è stato utilizzato largamente come
leggermente dolciastro. In passato è stato utilizzato largamente come refrigerante ma attualmente se ne evita l'uso a causa della sua
refrigerante ma attualmente se ne evita l'uso a causa della sua nocività.
nocività.
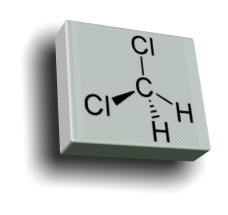
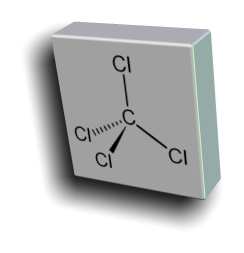
 Il diclorometano,o cloruro di metilene (DCM), è un composto chimico
Il diclorometano,o cloruro di metilene (DCM), è un composto chimico appartenente alla categoria degli alogenuri alchilici e largamente utilizzato come
solvente in chimica organica. A temperatura ambiente si presenta come un
liquido incolore e volatile dall'odore dolciastro. Data la sua volatilità e la sua
abilità di sciogliere un gran numero di composti organici, il diclorometano è un
solvente ideale per molti processi chimici e viene perciò largamente utilizzato per
la rimozione di vernice e grasso, per la decaffeinizzazione del caffè, per la
preparazione di estratti di luppolo ed altri aromi, come propellente spray per
aerosol e come agente schiumogeno per la preparazione di espansi poliuretanici.
appartenente alla categoria degli alogenuri alchilici e largamente utilizzato come
solvente in chimica organica. A temperatura ambiente si presenta come un
liquido incolore e volatile dall'odore dolciastro. Data la sua volatilità e la sua
abilità di sciogliere un gran numero di composti organici, il diclorometano è un
solvente ideale per molti processi chimici e viene perciò largamente utilizzato per
la rimozione di vernice e grasso, per la decaffeinizzazione del caffè, per la
preparazione di estratti di luppolo ed altri aromi, come propellente spray per
aerosol e come agente schiumogeno per la preparazione di espansi poliuretanici.
 Il triclorometano, detto anche cloroformio, è un alogenuro alchilico noto anche come
Il triclorometano, detto anche cloroformio, è un alogenuro alchilico noto anche come freon 20 o CFC 20. A temperatura ambiente è un liquido trasparente, abbastanza
freon 20 o CFC 20. A temperatura ambiente è un liquido trasparente, abbastanza volatile, dall'odore caratteristico. Non è infiammabile da solo, ma lo diventa se
volatile, dall'odore caratteristico. Non è infiammabile da solo, ma lo diventa se combinato con altri composti infiammabili. In passato il triclorometano era usato come
combinato con altri composti infiammabili. In passato il triclorometano era usato come anestetico in chirurgia e nelle preparazioni di sciroppi contro la tosse. Il principale
anestetico in chirurgia e nelle preparazioni di sciroppi contro la tosse. Il principale utilizzo del triclorometano è la produzione di freon R-22, usato come refrigerante,
utilizzo del triclorometano è la produzione di freon R-22, usato come refrigerante, anche se i freon sono stati messi internazionalmente al bando a causa del loro effetto
anche se i freon sono stati messi internazionalmente al bando a causa del loro effetto distruttivo sull'ozonosfera. Il triclorometano è usato anche come solvente nei laboratori,
distruttivo sull'ozonosfera. Il triclorometano è usato anche come solvente nei laboratori, anche se attualmente si tende a sostituirlo il più possibile con il cloruro di metilene. Il
anche se attualmente si tende a sostituirlo il più possibile con il cloruro di metilene. Il triclorometano reagisce con l'idrossido di sodio, preferibilmente in presenza di un
triclorometano reagisce con l'idrossido di sodio, preferibilmente in presenza di un catalizzatore di trasferimento di fase per la produzione del diclorocarbene che reagisce
catalizzatore di trasferimento di fase per la produzione del diclorocarbene che reagisce rapidamente con composti aromatici attivati (come i fenoli) producendo le
rapidamente con composti aromatici attivati (come i fenoli) producendo le corrispondenti aril-aldeidi (reazione di Reimer-Tiemann di idroformilazione). Il
corrispondenti aril-aldeidi (reazione di Reimer-Tiemann di idroformilazione). Il diclorocarbene può anche reagire con un alchene addizionandosi al doppio legame e
diclorocarbene può anche reagire con un alchene addizionandosi al doppio legame e producendo un diclorociclopropano sostituito. Il triclorometano deuterato, in cui al
producendo un diclorociclopropano sostituito. Il triclorometano deuterato, in cui al posto dell'atomo di idrogeno troviamo un atomo di deuterio, è comunemente usato
posto dell'atomo di idrogeno troviamo un atomo di deuterio, è comunemente usato come solvente nella spettroscopia di risonanza magnetica nucleare (NMR).
come solvente nella spettroscopia di risonanza magnetica nucleare (NMR). Il tetracloruro di carbonio, o tetraclorometano, è noto anche come freon
Il tetracloruro di carbonio, o tetraclorometano, è noto anche come freon 10 o CFC 10. A temperatura ambiente è un liquido apolare, volatile, dal
10 o CFC 10. A temperatura ambiente è un liquido apolare, volatile, dal caratteristico odore dolciastro, avvertibile anche a basse concentrazioni.
caratteristico odore dolciastro, avvertibile anche a basse concentrazioni. In passato è stato usato come solvente per il lavaggio a secco, per il
In passato è stato usato come solvente per il lavaggio a secco, per il rilevamento dei neutrini, negli estintori e come liquido di raffreddamento,
rilevamento dei neutrini, negli estintori e come liquido di raffreddamento, ma è stato via via sostituito da altri composti meno tossici. Prima della
ma è stato via via sostituito da altri composti meno tossici. Prima della stipula del protocollo di Montreal, grandi quantità di tetracloruro di
stipula del protocollo di Montreal, grandi quantità di tetracloruro di carbonio erano impiegate per produrre i freon R-11 e R-12, oggi in disuso
carbonio erano impiegate per produrre i freon R-11 e R-12, oggi in disuso per via del loro effetto deleterio sull'ozonosfera. Tuttavia è ancora
per via del loro effetto deleterio sull'ozonosfera. Tuttavia è ancora utilizzato per la produzione di freon meno distruttivi.
utilizzato per la produzione di freon meno distruttivi.
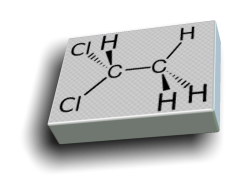
 Il dicloroetano, o cloruro di etilene, è un alogenuro alchilico che in passato
veniva chiamato anche "olio olandese" poiché fu sintetizzato per la prima
volta nel 1794 dalla Gezelschap der Hollandsche Scheikundigen (Società dei
chimici olandesi). A temperatura ambiente è un liquido incolore e oleoso
Il dicloroetano, o cloruro di etilene, è un alogenuro alchilico che in passato
veniva chiamato anche "olio olandese" poiché fu sintetizzato per la prima
volta nel 1794 dalla Gezelschap der Hollandsche Scheikundigen (Società dei
chimici olandesi). A temperatura ambiente è un liquido incolore e oleoso dall'odore penetrante di solvente. È molto infiammabile e durante la
dall'odore penetrante di solvente. È molto infiammabile e durante la combustione libera acido cloridrico e fosgene. Si ottiene per sintesi diretta,
miscelando etilene e cloro gassosi a temperatura e pressione standard ed
combustione libera acido cloridrico e fosgene. Si ottiene per sintesi diretta,
miscelando etilene e cloro gassosi a temperatura e pressione standard ed usando la luce o il cloruro ferrico come catalizzatori. Si usa perlopiù come
usando la luce o il cloruro ferrico come catalizzatori. Si usa perlopiù come intermedio nella sintesi del cloruro di vinile che è un precursore del PVC. È un
buon solvente apolare ed è usato come agente sgrassante, diluente per vernici
e come intermedio nella sintesi di molecole più complesse. In passato si usava
anche come antidetonante per carburanti insieme con il piombo tetraetile.
intermedio nella sintesi del cloruro di vinile che è un precursore del PVC. È un
buon solvente apolare ed è usato come agente sgrassante, diluente per vernici
e come intermedio nella sintesi di molecole più complesse. In passato si usava
anche come antidetonante per carburanti insieme con il piombo tetraetile.
 Il dicloropropano è un composto organico classificato come
Il dicloropropano è un composto organico classificato come clorocarburo. È un liquido incolore, infiammabile con un odore dolce
e si ottiene come sottoprodotto della produzione su larga scala di
clorocarburo. È un liquido incolore, infiammabile con un odore dolce
e si ottiene come sottoprodotto della produzione su larga scala di epicloridrina. Il dicloropropano è un intermedio nella produzione di
epicloridrina. Il dicloropropano è un intermedio nella produzione di percloroetilene e altre sostanze chimiche contenenti cloro. Un tempo
era utilizzata come fumigante per i terreni, come prodotto chimico
percloroetilene e altre sostanze chimiche contenenti cloro. Un tempo
era utilizzata come fumigante per i terreni, come prodotto chimico intermedio, come solvente industriale e nella produzione di
intermedio, come solvente industriale e nella produzione di svernicianti e vernici.
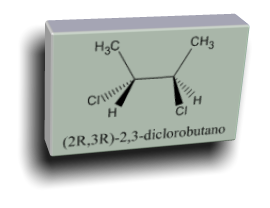
Il diclorobutano è un composto organico molto infiammabile, incolore,
svernicianti e vernici.
Il diclorobutano è un composto organico molto infiammabile, incolore, insolubile in acqua che si ottiene per reazione dell'acido cloridrico con
insolubile in acqua che si ottiene per reazione dell'acido cloridrico con tetraidrofurano ed è un intermedio nella sintesi dell'adiponitrile. Il
tetraidrofurano ed è un intermedio nella sintesi dell'adiponitrile. Il diclorobutano è un cloroalcano che racchiude molte sostanze sotto questo
diclorobutano è un cloroalcano che racchiude molte sostanze sotto questo nome generico (9 isomeri strutturali , di cui 5 hanno isomeri ottici). Essi
nome generico (9 isomeri strutturali , di cui 5 hanno isomeri ottici). Essi sono ottenuti con metodi di sintesi comuni per cloroalcani come la
sono ottenuti con metodi di sintesi comuni per cloroalcani come la clorurazione di radicali liberi di clorobutano o sostituzione nucleofila di
clorurazione di radicali liberi di clorobutano o sostituzione nucleofila di butandioli, a seconda l'isomero desiderato. Gli isomeri di diclorobutano
butandioli, a seconda l'isomero desiderato. Gli isomeri di diclorobutano sono ulteriormente utilizzati in varie sintesi organiche industriali e di
sono ulteriormente utilizzati in varie sintesi organiche industriali e di laboratorio, tra cui come precursore del nylon (via adiponitrile), per
laboratorio, tra cui come precursore del nylon (via adiponitrile), per l'ottenimento di tetraidrofurano (THF) e di cloroprene.
l'ottenimento di tetraidrofurano (THF) e di cloroprene. 
 Il clorobenzene, o benzene cloruro, è un composto chimico
Il clorobenzene, o benzene cloruro, è un composto chimico infiammabile derivato dal benzene, dove un atomo di idrogeno è
infiammabile derivato dal benzene, dove un atomo di idrogeno è sostituito da un atomo di cloro. A temperatura ambiente si presenta
sostituito da un atomo di cloro. A temperatura ambiente si presenta come un liquido incolore dall'odore caratteristico. Il clorobenzene
come un liquido incolore dall'odore caratteristico. Il clorobenzene viene prodotto come intermedio nella sintesi di pesticidi clorurati,
viene prodotto come intermedio nella sintesi di pesticidi clorurati, come il celebre DDT (dicloro-difenil-tricloroetano) o come solvente per
come il celebre DDT (dicloro-difenil-tricloroetano) o come solvente per la produzione di erbicidi, adesivi, vernici e come reagente di sintesi
la produzione di erbicidi, adesivi, vernici e come reagente di sintesi per altre sostanze. Il clorobenzene è prodotto anche
per altre sostanze. Il clorobenzene è prodotto anche dell'incenerimento dei rifiuti e dalla combustione incompleta di
dell'incenerimento dei rifiuti e dalla combustione incompleta di sostanze clorurate.
sostanze clorurate.













































































 © 2004 - 2015 Pianeta Marte.net - All right reserved
© 2004 - 2015 Pianeta Marte.net - All right reserved
 Sono quasi 40 anni ormai che si discute della missione VIKING ed in particolare degli esperimenti che avrebbero dovuto
Sono quasi 40 anni ormai che si discute della missione VIKING ed in particolare degli esperimenti che avrebbero dovuto provare o escludere la presenza di vita su Marte. Questi esperimenti erano concepiti per rilevare attività biologiche
provare o escludere la presenza di vita su Marte. Questi esperimenti erano concepiti per rilevare attività biologiche anche minime usando tre metodiche differenti, una delle quali (il labeled release (LR) o rilascio marcato) ha dato esiti
anche minime usando tre metodiche differenti, una delle quali (il labeled release (LR) o rilascio marcato) ha dato esiti decisamente positivi! Il Dottor Gilbert V. Levin, ideatore e curatore dell'esperimento LR, ha sempre sostenuto la positività degli
decisamente positivi! Il Dottor Gilbert V. Levin, ideatore e curatore dell'esperimento LR, ha sempre sostenuto la positività degli esiti dell'esperimento, in netto disaccordo con i vertici della NASA che invece hanno completamente rigettato ogni spiegazione di
esiti dell'esperimento, in netto disaccordo con i vertici della NASA che invece hanno completamente rigettato ogni spiegazione di tipo biologico a causa del mancato rilevamento di composti organici da parte del gascromatografo.
tipo biologico a causa del mancato rilevamento di composti organici da parte del gascromatografo. In realtà, con gli anni, saltò fuori che il gascromatografo aveva rilevato clorometano e diclorometano, ma che furono ritenuti
In realtà, con gli anni, saltò fuori che il gascromatografo aveva rilevato clorometano e diclorometano, ma che furono ritenuti una “contaminazione terrestre” dovuta probabilmente al detergente usato per sterilizzare le sonde. Vorrei far notare che tanto il
una “contaminazione terrestre” dovuta probabilmente al detergente usato per sterilizzare le sonde. Vorrei far notare che tanto il clorometano quanto il diclorometano sono estremamente volatili; come potevano essere sopravvissuti sulle sonde a parecchi
clorometano quanto il diclorometano sono estremamente volatili; come potevano essere sopravvissuti sulle sonde a parecchi mesi di viaggio nel vuoto cosmico???
mesi di viaggio nel vuoto cosmico??? Da notare anche il fatto dimostrato che copie di quel gascromatografo fallirono il rilevamento di composti organici anche su
Da notare anche il fatto dimostrato che copie di quel gascromatografo fallirono il rilevamento di composti organici anche su campioni terrestri a carica batterica conosciuta. Nonostante ciò, il mancato rilevamento di composti organici è rimasto fino ad
campioni terrestri a carica batterica conosciuta. Nonostante ciò, il mancato rilevamento di composti organici è rimasto fino ad oggi l'unico appiglio tecnico per annullare la validità dell'esito positivo dell'esperimento LR. Oltretutto anche gli altri due
oggi l'unico appiglio tecnico per annullare la validità dell'esito positivo dell'esperimento LR. Oltretutto anche gli altri due esperimenti biologici, lo scambio gassoso (Gas Exchange o GEX) e il rilascio pirolitico (Pyrolytic Release o PR), diedero esiti
esperimenti biologici, lo scambio gassoso (Gas Exchange o GEX) e il rilascio pirolitico (Pyrolytic Release o PR), diedero esiti interessanti tutt'altro che semplicemente negati, come invece affermano molti sedicenti “divulgatori”.
interessanti tutt'altro che semplicemente negati, come invece affermano molti sedicenti “divulgatori”. Per un'approfondita analisi dei tre esperimenti vi rimandiamo all'articolo: “Le sonde gemelle Viking trovarono la vita su
Per un'approfondita analisi dei tre esperimenti vi rimandiamo all'articolo: “Le sonde gemelle Viking trovarono la vita su Marte?”
Analizzando i vari punti in maniera indipendente si giunge alla conclusione che ci sia stata una volontà precisa di invalidare
Marte?”
Analizzando i vari punti in maniera indipendente si giunge alla conclusione che ci sia stata una volontà precisa di invalidare qualunque spiegazione di natura biologica a tutti i costi. E vediamo anche il perché. Lo scopo degli esperimenti biologici era che,
qualunque spiegazione di natura biologica a tutti i costi. E vediamo anche il perché. Lo scopo degli esperimenti biologici era che, almeno uno dei tre, risultasse positivo. Questa condizione è stata pienamente soddisfatta già dall'esperimento LR e parzialmente
almeno uno dei tre, risultasse positivo. Questa condizione è stata pienamente soddisfatta già dall'esperimento LR e parzialmente anche dagli esperimenti GEX e PR, raggiungendo così l'obiettivo primario preposto.
anche dagli esperimenti GEX e PR, raggiungendo così l'obiettivo primario preposto. Il gascromatografo rilevò clorometano e diclorometano nonostante la sua ridotta sensibilità; copie dello stesso strumento fallirono
Il gascromatografo rilevò clorometano e diclorometano nonostante la sua ridotta sensibilità; copie dello stesso strumento fallirono nel rilevamento di composti organici su campioni prelevati da alcuni deserti terrestri. Ciò significa che il livello di composti organici
nel rilevamento di composti organici su campioni prelevati da alcuni deserti terrestri. Ciò significa che il livello di composti organici sul suolo di Marte è maggiore di quello di alcuni deserti terrestri che comunque ospitano forme di vita. Nonostante ciò, si è
sul suolo di Marte è maggiore di quello di alcuni deserti terrestri che comunque ospitano forme di vita. Nonostante ciò, si è tentato in prima istanza di negare il rilevamento, salvo poi cercare di attribuirlo ad una contaminazione “terrestre”. Questa
tentato in prima istanza di negare il rilevamento, salvo poi cercare di attribuirlo ad una contaminazione “terrestre”. Questa argomentazione analizzata oggi risulta decisamente insostenibile. Intanto non mi risulta che il clorometano e il diclorometano
argomentazione analizzata oggi risulta decisamente insostenibile. Intanto non mi risulta che il clorometano e il diclorometano vengano usati come detergenti o sterilizzanti. Ammesso e non concesso che questi composti fossero presenti al momento del
vengano usati come detergenti o sterilizzanti. Ammesso e non concesso che questi composti fossero presenti al momento del lancio, avrebbero dovuto disperdersi completamente durante il viaggio di andata verso Marte.
lancio, avrebbero dovuto disperdersi completamente durante il viaggio di andata verso Marte. Anche ammettendo la possibilità che una qualche quantità di contaminante sia rimasta sulla sonda, sopravvivendo al viaggio,
Anche ammettendo la possibilità che una qualche quantità di contaminante sia rimasta sulla sonda, sopravvivendo al viaggio, quest’ultima avrebbe dovuto diminuire ad ogni successiva analisi di un nuovo campione. Immaginiamo per esempio di usare un
quest’ultima avrebbe dovuto diminuire ad ogni successiva analisi di un nuovo campione. Immaginiamo per esempio di usare un cucchiaino sporco di miele per raccogliere del sale; la prima cucchiaiata sarà sicuramente la più “sporca” ma, man mano che
cucchiaino sporco di miele per raccogliere del sale; la prima cucchiaiata sarà sicuramente la più “sporca” ma, man mano che andiamo avanti, il cucchiaino stesso tenderà a perdere lo strato di miele fino a rimanere pressoché pulito. Quindi, la “scusa” della
andiamo avanti, il cucchiaino stesso tenderà a perdere lo strato di miele fino a rimanere pressoché pulito. Quindi, la “scusa” della contaminazione terrestre non è per nulla convincente in quanto avrebbero potuto discriminarla ripetendo più volte l'analisi. Risulta
contaminazione terrestre non è per nulla convincente in quanto avrebbero potuto discriminarla ripetendo più volte l'analisi. Risulta quindi evidente la volontà di utilizzare l'esperimento col gascromatografo per invalidare gli altri tre. Infatti per sostenere questa
quindi evidente la volontà di utilizzare l'esperimento col gascromatografo per invalidare gli altri tre. Infatti per sostenere questa debole tesi si è ricorso a spiegazioni fantasiose come la pioggia di super ossidi che avrebbero così sterilizzato continuamente la
debole tesi si è ricorso a spiegazioni fantasiose come la pioggia di super ossidi che avrebbero così sterilizzato continuamente la superficie marziana nonostante gli apporti meteorici. E infatti ben noto che una costante pioggia di meteoriti e comete fornisce un
superficie marziana nonostante gli apporti meteorici. E infatti ben noto che una costante pioggia di meteoriti e comete fornisce un costante apporto di composti organici alla superficie marziana. Inutile aggiungere che ne acqua ossigenata ne qualsivoglia sorta
costante apporto di composti organici alla superficie marziana. Inutile aggiungere che ne acqua ossigenata ne qualsivoglia sorta di super ossido è mai stato identificato sulla superficie marziana.
di super ossido è mai stato identificato sulla superficie marziana. Ci troviamo quindi di fronte ad una serie di teorie farlocche e mai dimostrate che hanno tenuto banco fino ai giorni nostri a
Ci troviamo quindi di fronte ad una serie di teorie farlocche e mai dimostrate che hanno tenuto banco fino ai giorni nostri a sostegno della tesi che la superficie di Marte fosse completamente sterile e priva di composti organici, oltreché estremamente
sostegno della tesi che la superficie di Marte fosse completamente sterile e priva di composti organici, oltreché estremamente ossidante. Una teoria contro dei fatti oggettivi; questo è ciò che la NASA ha usato contro le tesi del dr. Levin. Nessun metodo
ossidante. Una teoria contro dei fatti oggettivi; questo è ciò che la NASA ha usato contro le tesi del dr. Levin. Nessun metodo scientifico può essere invocato a sostegno di questo modus operandi; un esperimento che si prefigge determinati scopi e che li
scientifico può essere invocato a sostegno di questo modus operandi; un esperimento che si prefigge determinati scopi e che li raggiunge è universalmente riconosciuto come “esito positivo”.
raggiunge è universalmente riconosciuto come “esito positivo”.  Per i più coriacei viene in aiuto la missione MSL Curiosity, la quale ha rilevato sia i composti già trovati dalle Viking che una bella
Per i più coriacei viene in aiuto la missione MSL Curiosity, la quale ha rilevato sia i composti già trovati dalle Viking che una bella sfilza di idrocarburi! Come la mettiamo adesso?? Rimarremo tutti devoti alla “Santa Madre NASA” o decideremo finalmente di
sfilza di idrocarburi! Come la mettiamo adesso?? Rimarremo tutti devoti alla “Santa Madre NASA” o decideremo finalmente di aprire gli occhi e accendere i neuroni?
aprire gli occhi e accendere i neuroni?  Ecco una breve descrizione dei composti organici rilevati:
Vista la varietà di composti organici rilevati, vorrei far notare quanto fosse insulsa la teoria dei “Super ossidi” che avrebbero
Ecco una breve descrizione dei composti organici rilevati:
Vista la varietà di composti organici rilevati, vorrei far notare quanto fosse insulsa la teoria dei “Super ossidi” che avrebbero distrutto anche quel po' di composti organici che arrivavano dallo spazio. Visto che anche sulla Luna sono presenti un minimo di
distrutto anche quel po' di composti organici che arrivavano dallo spazio. Visto che anche sulla Luna sono presenti un minimo di composti organici, giustificare la loro totale assenza dalla superficie di Marte ha richiesto veramente un colpo di genio
composti organici, giustificare la loro totale assenza dalla superficie di Marte ha richiesto veramente un colpo di genio eccezionale!
eccezionale! In un documento pubblicato dalla NASA il 30 dicembre 1979 intitolato “Viking magnetic properties experiment - Extended mission
In un documento pubblicato dalla NASA il 30 dicembre 1979 intitolato “Viking magnetic properties experiment - Extended mission results”, disponibile all'indirizzo http://ntrs.nasa.gov/search.jsp?R=19800042219 , si legge:
results”, disponibile all'indirizzo http://ntrs.nasa.gov/search.jsp?R=19800042219 , si legge: “I magneti del retroescavatore sul Viking Lander (VL) 2 furono puliti con successo, in seguito fu eseguito un test praticando
“I magneti del retroescavatore sul Viking Lander (VL) 2 furono puliti con successo, in seguito fu eseguito un test praticando interramenti successivi del retroescavatore pulito nella superficie. La rapida saturazione dei magneti ha confermato le prove
interramenti successivi del retroescavatore pulito nella superficie. La rapida saturazione dei magneti ha confermato le prove risultanti dalla missione primaria, cioè che il minerale magnetico nella superficie marziana è ampiamente distribuito,
risultanti dalla missione primaria, cioè che il minerale magnetico nella superficie marziana è ampiamente distribuito, probabilmente in forma di particelle miste di minerali magnetici e non magnetici. Un'immagine del retroescavatore del VL 2 prese
probabilmente in forma di particelle miste di minerali magnetici e non magnetici. Un'immagine del retroescavatore del VL 2 prese con lo specchio di ingrandimento X4 dimostra la natura granulare del materiale magnetico attratto. La presenza di maghemite e
con lo specchio di ingrandimento X4 dimostra la natura granulare del materiale magnetico attratto. La presenza di maghemite e la sua comparsa come parte del pigmento, o come sottile rivestimento, in tutte le particelle minerali, o nei cristalliti discretamente
la sua comparsa come parte del pigmento, o come sottile rivestimento, in tutte le particelle minerali, o nei cristalliti discretamente e finemente suddivisi e diffusi, sono coerenti con i dati provenienti dagli esperimenti di analisi inorganica e simulazioni di
e finemente suddivisi e diffusi, sono coerenti con i dati provenienti dagli esperimenti di analisi inorganica e simulazioni di laboratorio dei risultati degli esperimenti biologici compiuti su Marte.”.
Il Dottor Levin ha fatto notare in diverse pubblicazioni l'incompatibilità della presenza di materiale magnetizzato con un suolo
laboratorio dei risultati degli esperimenti biologici compiuti su Marte.”.
Il Dottor Levin ha fatto notare in diverse pubblicazioni l'incompatibilità della presenza di materiale magnetizzato con un suolo fortemente ossidante. Un suolo fortemente ossidante distruggerebbe ogni traccia di materiale magnetico che quindi non avrebbe
fortemente ossidante. Un suolo fortemente ossidante distruggerebbe ogni traccia di materiale magnetico che quindi non avrebbe potuto essere catturato dai magneti a bordo del VL2!
potuto essere catturato dai magneti a bordo del VL2! Ma non basta; il clorometano e il diclorometano rilevati dal gascromatografo erano anch'essi incompatibili con un suolo
Ma non basta; il clorometano e il diclorometano rilevati dal gascromatografo erano anch'essi incompatibili con un suolo fortemente ossidante, tanto più se fossero realmente stati un residuo del detergente usato per sterilizzare i due landers! Infatti un
fortemente ossidante, tanto più se fossero realmente stati un residuo del detergente usato per sterilizzare i due landers! Infatti un terreno fortemente ossidante avrebbe distrutto i due composti prima ancora che il gascromatografo iniziasse a scaldare i
terreno fortemente ossidante avrebbe distrutto i due composti prima ancora che il gascromatografo iniziasse a scaldare i campioni di suolo stesso! È totalmente illogico pensare che un terreno in grado di aggredire e distruggere qualunque composto
campioni di suolo stesso! È totalmente illogico pensare che un terreno in grado di aggredire e distruggere qualunque composto organico proveniente dallo spazio non sia poi in grado di distruggere le deboli tracce lasciate da un detergente!
organico proveniente dallo spazio non sia poi in grado di distruggere le deboli tracce lasciate da un detergente!  Per decenni, schiere di giornalisti scientifici e divulgatori, hanno strombazzato la negatività degli esperimenti biologici compiuti
Per decenni, schiere di giornalisti scientifici e divulgatori, hanno strombazzato la negatività degli esperimenti biologici compiuti dalle sonde Viking, senza mai entrare minimamente nel dettaglio dei singoli esperimenti e senza mai palesare il benché minimo
dalle sonde Viking, senza mai entrare minimamente nel dettaglio dei singoli esperimenti e senza mai palesare il benché minimo dubbio al riguardo! È questo il modo di fare giornalismo??? Riportare una notizia senza un minimo di verifica??? Si fa un gran
dubbio al riguardo! È questo il modo di fare giornalismo??? Riportare una notizia senza un minimo di verifica??? Si fa un gran parlare di par condicio, ma chi di voi “Giornalari scientifici” si è mai sognato di esporre anche la tesi del Dottor Gilbert V. Levin in
parlare di par condicio, ma chi di voi “Giornalari scientifici” si è mai sognato di esporre anche la tesi del Dottor Gilbert V. Levin in contrapposizione a quella della NASA???
contrapposizione a quella della NASA??? Ultima, ma non per importanza, la questione del metano su Marte come ulteriore prova a sostegno della tesi della vita su Marte.
Ultima, ma non per importanza, la questione del metano su Marte come ulteriore prova a sostegno della tesi della vita su Marte. C'è chi sostiene la sua origine biologica e chi sostiene l'origine geologica o abiogenica, senza di fatto arrivare ad una
C'è chi sostiene la sua origine biologica e chi sostiene l'origine geologica o abiogenica, senza di fatto arrivare ad una conclusione!
conclusione! Ancora una volta, nessuno ci spiega che il vero problema non è da dove arriva il metano ma piuttosto come fa a sparire
Ancora una volta, nessuno ci spiega che il vero problema non è da dove arriva il metano ma piuttosto come fa a sparire così velocemente!! Infatti è stato dimostrato che il metano dovrebbe resistere circa 300 anni nell'atmosfera marziana prima di
così velocemente!! Infatti è stato dimostrato che il metano dovrebbe resistere circa 300 anni nell'atmosfera marziana prima di disgregarsi e/o reagire con altre sostanze; ma allora come mai lo si vede sparire nell'arco di mesi, a volte settimane o addirittura
disgregarsi e/o reagire con altre sostanze; ma allora come mai lo si vede sparire nell'arco di mesi, a volte settimane o addirittura giorni? Cos'è in grado di distruggere grandi quantità di metano in così poco tempo?
giorni? Cos'è in grado di distruggere grandi quantità di metano in così poco tempo? Ovviamente nessuno si azzarda a sollevare la questione, visto che in questo caso non ci sarebbero le due classiche fazioni
Ovviamente nessuno si azzarda a sollevare la questione, visto che in questo caso non ci sarebbero le due classiche fazioni opposte da lasciare scannare eternamente l'una contro l'altra ma solo un'unica risposta: batteri metanotrofi!!! Proprio così,
opposte da lasciare scannare eternamente l'una contro l'altra ma solo un'unica risposta: batteri metanotrofi!!! Proprio così, perché tutti i processi chimico-fisici conosciuti in grado di distruggere il metano eventualmente immesso nell'atmosfera marziana,
perché tutti i processi chimico-fisici conosciuti in grado di distruggere il metano eventualmente immesso nell'atmosfera marziana, anche se sommati insieme, non riescono far prima dei 300 anni citati prima, quindi in questo caso non ci si può appellare ad altro
anche se sommati insieme, non riescono far prima dei 300 anni citati prima, quindi in questo caso non ci si può appellare ad altro se non ai batteri metanotrofi, ovvero batteri che si nutrono di metano.
se non ai batteri metanotrofi, ovvero batteri che si nutrono di metano. Non credo proprio che simili osservazioni potranno giungere facilmente all'attenzione dell'opinione pubblica, visto che i Media
Non credo proprio che simili osservazioni potranno giungere facilmente all'attenzione dell'opinione pubblica, visto che i Media preferiscono dedicarsi servilmente a propagandare le sole versioni “ufficiali” somministrate dalla NASA e dall'ESA in maniera
preferiscono dedicarsi servilmente a propagandare le sole versioni “ufficiali” somministrate dalla NASA e dall'ESA in maniera totalmente acritica!!! Vorrei tanto avere la possibilità di intervistare pubblicamente almeno uno di quei “geni” che per decenni
totalmente acritica!!! Vorrei tanto avere la possibilità di intervistare pubblicamente almeno uno di quei “geni” che per decenni hanno tenuto banco con le loro teorie assurde come quella dei super ossidi! Evidentemente loro hanno scoperto il vaccino contro
hanno tenuto banco con le loro teorie assurde come quella dei super ossidi! Evidentemente loro hanno scoperto il vaccino contro la vergogna... che magari viene proprio da Marte!
la vergogna... che magari viene proprio da Marte! Pubblicazioni ufficiali di riferimento:
2014 "MARS: Dead or Alive?" Gilbert V. Levin, Arizona State University and Patricia Ann Straat NIH (Ret.) Presented at Mars
Pubblicazioni ufficiali di riferimento:
2014 "MARS: Dead or Alive?" Gilbert V. Levin, Arizona State University and Patricia Ann Straat NIH (Ret.) Presented at Mars Society Convention, League City, TX, August 8, 2014
Society Convention, League City, TX, August 8, 2014 2015 "Mars methane detection and variability at Gale crater" Christopher R. Webster, Paul R. Mahaffy, Sushil K. Atreya, Gregory
2015 "Mars methane detection and variability at Gale crater" Christopher R. Webster, Paul R. Mahaffy, Sushil K. Atreya, Gregory J. Flesch, Michael A. Mischna, Pierre-Yves Meslin, Kenneth A. Farley, Pamela G. Conrad, Lance E. Christensen, Alexander A.
J. Flesch, Michael A. Mischna, Pierre-Yves Meslin, Kenneth A. Farley, Pamela G. Conrad, Lance E. Christensen, Alexander A. Pavlov, Javier Martín-Torres,, María-Paz Zorzano, Timothy H. McConnochie, Tobias Owen, Jennifer L. Eigenbrode, Daniel P.
Pavlov, Javier Martín-Torres,, María-Paz Zorzano, Timothy H. McConnochie, Tobias Owen, Jennifer L. Eigenbrode, Daniel P. Glavin, Andrew Steele, Charles A. Malespin, P. Douglas Archer Jr., Brad Sutter, Patrice Coll, Caroline Freissinet, Christopher P.
Glavin, Andrew Steele, Charles A. Malespin, P. Douglas Archer Jr., Brad Sutter, Patrice Coll, Caroline Freissinet, Christopher P. McKay, John E. Moores, Susanne P. Schwenzer, John C. Bridges, Rafael Navarro-Gonzalez, Ralf Gellert, Mark T. Lemmon, the
McKay, John E. Moores, Susanne P. Schwenzer, John C. Bridges, Rafael Navarro-Gonzalez, Ralf Gellert, Mark T. Lemmon, the MSL Science Team
MSL Science Team 2014 "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D. P. Glavin, P. R.
2014 "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D. P. Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et
Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et al.
al. 2014 "Volatile and Organic Compositions of Sedimentary Rocks in Yellowknife Bay, Gale Crater, Mars" D. W. Ming, P. D. Archer
2014 "Volatile and Organic Compositions of Sedimentary Rocks in Yellowknife Bay, Gale Crater, Mars" D. W. Ming, P. D. Archer Jr., D. P. Glavin, J. L. Eigenbrode, H. B. Franz, B. Sutter, A. E. Brunner, J. C. Stern, C. Freissinet, A. C. McAdam, P. R. Mahaffy,
Jr., D. P. Glavin, J. L. Eigenbrode, H. B. Franz, B. Sutter, A. E. Brunner, J. C. Stern, C. Freissinet, A. C. McAdam, P. R. Mahaffy, M. Cabane, P. Coll, J. L. Campbell, S. K. Atreya, P. B. Niles, J. F. Bell III, D. L. Bish, W. B. Brinckerhoff, A. Buch, P. G. Conrad,
M. Cabane, P. Coll, J. L. Campbell, S. K. Atreya, P. B. Niles, J. F. Bell III, D. L. Bish, W. B. Brinckerhoff, A. Buch, P. G. Conrad, D. J. Des Marais, B. L. Ehlmann, A. G. Fairén, K. Farley, G. J. Flesch, P. Francois, R. Gellert, J. A. Grant, J. P. Grotzinger, S.
D. J. Des Marais, B. L. Ehlmann, A. G. Fairén, K. Farley, G. J. Flesch, P. Francois, R. Gellert, J. A. Grant, J. P. Grotzinger, S. Gupta, K. E. Herkenhoff, J. A. Hurowitz, L. A. Leshin, K. W. Lewis, S. M. McLennan, K. E. Miller, J. Moersch, R. V. Morris, R.
Gupta, K. E. Herkenhoff, J. A. Hurowitz, L. A. Leshin, K. W. Lewis, S. M. McLennan, K. E. Miller, J. Moersch, R. V. Morris, R. Navarro-González, A. A. Pavlov, G. M. Perrett, I. Pradler, S. W. Squyres, R. E. Summons, A. Steele, E. M. Stolper, D. Y.
Navarro-González, A. A. Pavlov, G. M. Perrett, I. Pradler, S. W. Squyres, R. E. Summons, A. Steele, E. M. Stolper, D. Y. Sumner, C. Szopa, S. Teinturier, M. G. Trainer, A. H. Treiman, D. T. Vaniman, A. R. Vasavada, C. R. Webster, J. J. Wray, R. A.
Sumner, C. Szopa, S. Teinturier, M. G. Trainer, A. H. Treiman, D. T. Vaniman, A. R. Vasavada, C. R. Webster, J. J. Wray, R. A. Yingst, MSL Science Team
Yingst, MSL Science Team 2010 "Reanalysis of the Viking results suggests perchlorate and organics at midlatitudes on Mars" Rafael Navarro‐González,
2010 "Reanalysis of the Viking results suggests perchlorate and organics at midlatitudes on Mars" Rafael Navarro‐González, Edgar Vargas, José de la Rosa, Alejandro C. Raga, and Christopher P. McKay
Edgar Vargas, José de la Rosa, Alejandro C. Raga, and Christopher P. McKay

 Gascromatogramma del campione CB-3.
Gascromatogramma del campione CB-3.  1: clorometano, 2: diclorometano, 3: triclorometano, 4: tetracloruro di carbonio, 5: dicloroetane, 6: dicloropropano,
1: clorometano, 2: diclorometano, 3: triclorometano, 4: tetracloruro di carbonio, 5: dicloroetane, 6: dicloropropano,  7: diclorobutano, 8: clorobenzene.
7: diclorobutano, 8: clorobenzene. Tratto da "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D.P.
Tratto da "ORGANIC MOLECULES IN THE SHEEPBED MUDSTONE, GALE CRATER, MARS." C. Freissinet, D.P. Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B.
Glavin, P. R. Mahaffy, K. E. Miller, J. L. Eigenbrode, R. E. Summons, A. E. Brunner, A. Buch, C. Szopa, P. D. Archer, H. B. Franz, A. Steele et al.
Franz, A. Steele et al.










 Il clorometano, detto anche metilcloruro o cloruro di metile (o con le
Il clorometano, detto anche metilcloruro o cloruro di metile (o con le sigle R-40 e HCC 40), è un composto chimico che si presenta sotto
sigle R-40 e HCC 40), è un composto chimico che si presenta sotto forma di gas incolore, infiammabile e caratterizzato da un odore
forma di gas incolore, infiammabile e caratterizzato da un odore leggermente dolciastro. In passato è stato utilizzato largamente come
leggermente dolciastro. In passato è stato utilizzato largamente come refrigerante ma attualmente se ne evita l'uso a causa della sua
refrigerante ma attualmente se ne evita l'uso a causa della sua nocività.
nocività.
 Il diclorometano,o cloruro di metilene (DCM), è un composto chimico
Il diclorometano,o cloruro di metilene (DCM), è un composto chimico appartenente alla categoria degli alogenuri alchilici e largamente utilizzato come
solvente in chimica organica. A temperatura ambiente si presenta come un
liquido incolore e volatile dall'odore dolciastro. Data la sua volatilità e la sua
abilità di sciogliere un gran numero di composti organici, il diclorometano è un
solvente ideale per molti processi chimici e viene perciò largamente utilizzato per
la rimozione di vernice e grasso, per la decaffeinizzazione del caffè, per la
preparazione di estratti di luppolo ed altri aromi, come propellente spray per
aerosol e come agente schiumogeno per la preparazione di espansi poliuretanici.
appartenente alla categoria degli alogenuri alchilici e largamente utilizzato come
solvente in chimica organica. A temperatura ambiente si presenta come un
liquido incolore e volatile dall'odore dolciastro. Data la sua volatilità e la sua
abilità di sciogliere un gran numero di composti organici, il diclorometano è un
solvente ideale per molti processi chimici e viene perciò largamente utilizzato per
la rimozione di vernice e grasso, per la decaffeinizzazione del caffè, per la
preparazione di estratti di luppolo ed altri aromi, come propellente spray per
aerosol e come agente schiumogeno per la preparazione di espansi poliuretanici.
 Il triclorometano, detto anche cloroformio, è un alogenuro alchilico noto anche come
Il triclorometano, detto anche cloroformio, è un alogenuro alchilico noto anche come freon 20 o CFC 20. A temperatura ambiente è un liquido trasparente, abbastanza
freon 20 o CFC 20. A temperatura ambiente è un liquido trasparente, abbastanza volatile, dall'odore caratteristico. Non è infiammabile da solo, ma lo diventa se
volatile, dall'odore caratteristico. Non è infiammabile da solo, ma lo diventa se combinato con altri composti infiammabili. In passato il triclorometano era usato come
combinato con altri composti infiammabili. In passato il triclorometano era usato come anestetico in chirurgia e nelle preparazioni di sciroppi contro la tosse. Il principale
anestetico in chirurgia e nelle preparazioni di sciroppi contro la tosse. Il principale utilizzo del triclorometano è la produzione di freon R-22, usato come refrigerante,
utilizzo del triclorometano è la produzione di freon R-22, usato come refrigerante, anche se i freon sono stati messi internazionalmente al bando a causa del loro effetto
anche se i freon sono stati messi internazionalmente al bando a causa del loro effetto distruttivo sull'ozonosfera. Il triclorometano è usato anche come solvente nei laboratori,
distruttivo sull'ozonosfera. Il triclorometano è usato anche come solvente nei laboratori, anche se attualmente si tende a sostituirlo il più possibile con il cloruro di metilene. Il
anche se attualmente si tende a sostituirlo il più possibile con il cloruro di metilene. Il triclorometano reagisce con l'idrossido di sodio, preferibilmente in presenza di un
triclorometano reagisce con l'idrossido di sodio, preferibilmente in presenza di un catalizzatore di trasferimento di fase per la produzione del diclorocarbene che reagisce
catalizzatore di trasferimento di fase per la produzione del diclorocarbene che reagisce rapidamente con composti aromatici attivati (come i fenoli) producendo le
rapidamente con composti aromatici attivati (come i fenoli) producendo le corrispondenti aril-aldeidi (reazione di Reimer-Tiemann di idroformilazione). Il
corrispondenti aril-aldeidi (reazione di Reimer-Tiemann di idroformilazione). Il diclorocarbene può anche reagire con un alchene addizionandosi al doppio legame e
diclorocarbene può anche reagire con un alchene addizionandosi al doppio legame e producendo un diclorociclopropano sostituito. Il triclorometano deuterato, in cui al
producendo un diclorociclopropano sostituito. Il triclorometano deuterato, in cui al posto dell'atomo di idrogeno troviamo un atomo di deuterio, è comunemente usato
posto dell'atomo di idrogeno troviamo un atomo di deuterio, è comunemente usato come solvente nella spettroscopia di risonanza magnetica nucleare (NMR).
come solvente nella spettroscopia di risonanza magnetica nucleare (NMR). Il tetracloruro di carbonio, o tetraclorometano, è noto anche come freon
Il tetracloruro di carbonio, o tetraclorometano, è noto anche come freon 10 o CFC 10. A temperatura ambiente è un liquido apolare, volatile, dal
10 o CFC 10. A temperatura ambiente è un liquido apolare, volatile, dal caratteristico odore dolciastro, avvertibile anche a basse concentrazioni.
caratteristico odore dolciastro, avvertibile anche a basse concentrazioni. In passato è stato usato come solvente per il lavaggio a secco, per il
In passato è stato usato come solvente per il lavaggio a secco, per il rilevamento dei neutrini, negli estintori e come liquido di raffreddamento,
rilevamento dei neutrini, negli estintori e come liquido di raffreddamento, ma è stato via via sostituito da altri composti meno tossici. Prima della
ma è stato via via sostituito da altri composti meno tossici. Prima della stipula del protocollo di Montreal, grandi quantità di tetracloruro di
stipula del protocollo di Montreal, grandi quantità di tetracloruro di carbonio erano impiegate per produrre i freon R-11 e R-12, oggi in disuso
carbonio erano impiegate per produrre i freon R-11 e R-12, oggi in disuso per via del loro effetto deleterio sull'ozonosfera. Tuttavia è ancora
per via del loro effetto deleterio sull'ozonosfera. Tuttavia è ancora utilizzato per la produzione di freon meno distruttivi.
utilizzato per la produzione di freon meno distruttivi.
 Il dicloroetano, o cloruro di etilene, è un alogenuro alchilico che in passato
veniva chiamato anche "olio olandese" poiché fu sintetizzato per la prima
volta nel 1794 dalla Gezelschap der Hollandsche Scheikundigen (Società dei
chimici olandesi). A temperatura ambiente è un liquido incolore e oleoso
Il dicloroetano, o cloruro di etilene, è un alogenuro alchilico che in passato
veniva chiamato anche "olio olandese" poiché fu sintetizzato per la prima
volta nel 1794 dalla Gezelschap der Hollandsche Scheikundigen (Società dei
chimici olandesi). A temperatura ambiente è un liquido incolore e oleoso dall'odore penetrante di solvente. È molto infiammabile e durante la
dall'odore penetrante di solvente. È molto infiammabile e durante la combustione libera acido cloridrico e fosgene. Si ottiene per sintesi diretta,
miscelando etilene e cloro gassosi a temperatura e pressione standard ed
combustione libera acido cloridrico e fosgene. Si ottiene per sintesi diretta,
miscelando etilene e cloro gassosi a temperatura e pressione standard ed usando la luce o il cloruro ferrico come catalizzatori. Si usa perlopiù come
usando la luce o il cloruro ferrico come catalizzatori. Si usa perlopiù come intermedio nella sintesi del cloruro di vinile che è un precursore del PVC. È un
buon solvente apolare ed è usato come agente sgrassante, diluente per vernici
e come intermedio nella sintesi di molecole più complesse. In passato si usava
anche come antidetonante per carburanti insieme con il piombo tetraetile.
intermedio nella sintesi del cloruro di vinile che è un precursore del PVC. È un
buon solvente apolare ed è usato come agente sgrassante, diluente per vernici
e come intermedio nella sintesi di molecole più complesse. In passato si usava
anche come antidetonante per carburanti insieme con il piombo tetraetile.
 Il dicloropropano è un composto organico classificato come
Il dicloropropano è un composto organico classificato come clorocarburo. È un liquido incolore, infiammabile con un odore dolce
e si ottiene come sottoprodotto della produzione su larga scala di
clorocarburo. È un liquido incolore, infiammabile con un odore dolce
e si ottiene come sottoprodotto della produzione su larga scala di epicloridrina. Il dicloropropano è un intermedio nella produzione di
epicloridrina. Il dicloropropano è un intermedio nella produzione di percloroetilene e altre sostanze chimiche contenenti cloro. Un tempo
era utilizzata come fumigante per i terreni, come prodotto chimico
percloroetilene e altre sostanze chimiche contenenti cloro. Un tempo
era utilizzata come fumigante per i terreni, come prodotto chimico intermedio, come solvente industriale e nella produzione di
intermedio, come solvente industriale e nella produzione di svernicianti e vernici.
Il diclorobutano è un composto organico molto infiammabile, incolore,
svernicianti e vernici.
Il diclorobutano è un composto organico molto infiammabile, incolore, insolubile in acqua che si ottiene per reazione dell'acido cloridrico con
insolubile in acqua che si ottiene per reazione dell'acido cloridrico con tetraidrofurano ed è un intermedio nella sintesi dell'adiponitrile. Il
tetraidrofurano ed è un intermedio nella sintesi dell'adiponitrile. Il diclorobutano è un cloroalcano che racchiude molte sostanze sotto questo
diclorobutano è un cloroalcano che racchiude molte sostanze sotto questo nome generico (9 isomeri strutturali , di cui 5 hanno isomeri ottici). Essi
nome generico (9 isomeri strutturali , di cui 5 hanno isomeri ottici). Essi sono ottenuti con metodi di sintesi comuni per cloroalcani come la
sono ottenuti con metodi di sintesi comuni per cloroalcani come la clorurazione di radicali liberi di clorobutano o sostituzione nucleofila di
clorurazione di radicali liberi di clorobutano o sostituzione nucleofila di butandioli, a seconda l'isomero desiderato. Gli isomeri di diclorobutano
butandioli, a seconda l'isomero desiderato. Gli isomeri di diclorobutano sono ulteriormente utilizzati in varie sintesi organiche industriali e di
sono ulteriormente utilizzati in varie sintesi organiche industriali e di laboratorio, tra cui come precursore del nylon (via adiponitrile), per
laboratorio, tra cui come precursore del nylon (via adiponitrile), per l'ottenimento di tetraidrofurano (THF) e di cloroprene.
l'ottenimento di tetraidrofurano (THF) e di cloroprene. 
 Il clorobenzene, o benzene cloruro, è un composto chimico
Il clorobenzene, o benzene cloruro, è un composto chimico infiammabile derivato dal benzene, dove un atomo di idrogeno è
infiammabile derivato dal benzene, dove un atomo di idrogeno è sostituito da un atomo di cloro. A temperatura ambiente si presenta
sostituito da un atomo di cloro. A temperatura ambiente si presenta come un liquido incolore dall'odore caratteristico. Il clorobenzene
come un liquido incolore dall'odore caratteristico. Il clorobenzene viene prodotto come intermedio nella sintesi di pesticidi clorurati,
viene prodotto come intermedio nella sintesi di pesticidi clorurati, come il celebre DDT (dicloro-difenil-tricloroetano) o come solvente per
come il celebre DDT (dicloro-difenil-tricloroetano) o come solvente per la produzione di erbicidi, adesivi, vernici e come reagente di sintesi
la produzione di erbicidi, adesivi, vernici e come reagente di sintesi per altre sostanze. Il clorobenzene è prodotto anche
per altre sostanze. Il clorobenzene è prodotto anche dell'incenerimento dei rifiuti e dalla combustione incompleta di
dell'incenerimento dei rifiuti e dalla combustione incompleta di sostanze clorurate.
sostanze clorurate.